Aperçu
- Autre dénomination : RPC-1063
- Compagnie pharmaceutique : Celgene
- Voie d’administration : orale (0,5 mg ou 1 mg par jour)
- Classe thérapeutique : modulateur des récepteurs de la sphingosine-1-phosphate (S1P); immunomodulateur
- Traitement émergent contre la SP cyclique
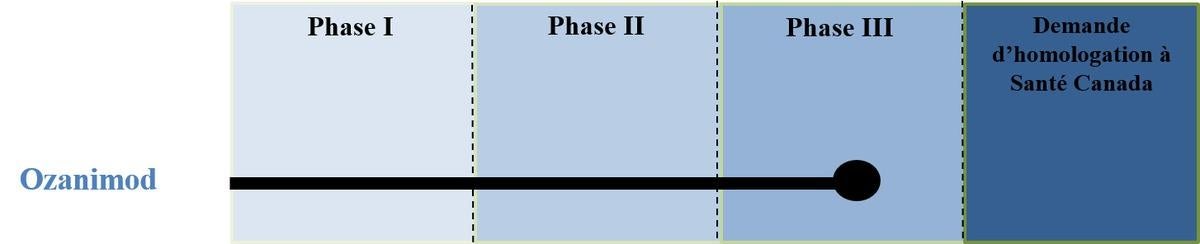
- Statut : essai clinique de phase III achevé; étude de prolongation en cours
Mode d’action
L’ozanimod (aussi appelé RPC-1063) pénètre dans le système nerveux central (SNC) et se lie à certains sous-types de récepteur de la sphingosine-1-phosphate (S1P), soit les récepteurs S1P1R et S1P5R. On trouve les récepteurs de la S1P à la surface de certaines cellules immunitaires, à savoir les lymphocytes T et les lymphocytes B, qui jouent un rôle dans la formation des lésions qui touchent le SNC dans le contexte de la SP. En se liant aux récepteurs de la S1P, l’ozanimod prévient l’activation de ces cellules nocives, plus particulièrement les lymphocytes B et les lymphocytes T, et leur libération subséquente, à partir des ganglions lymphatiques et du thymus, dans la circulation sanguine, puis dans le cerveau et la moelle épinière. Il a été démontré que l’ozanimod réduit l’inflammation chez des animaux atteints d’une maladie semblable à la SP.
Travaux de recherche et résultats
Étude RADIANCE : essais cliniques de phases II et III
Un essai clinique comparatif avec placebo de phase II, à double insu et à répartition aléatoire, baptisé RADIANCE, a permis d’évaluer l’efficacité et l’innocuité de l’ozanimod chez 258 personnes atteintes de SP cyclique (poussées-rémissions). Durant 24 semaines, les participants à cette étude ont reçu par voie orale une dose quotidienne d’ozanimod (0,5 mg ou 1 mg) ou un placebo. Les auteurs de l’essai RADIANCE ont pu alors constater que l’ozanimod avait satisfait au paramètre d’évaluation principal, lequel consistait en la réduction du nombre de lésions entre la 12e et la 24e semaine de traitement par ce médicament, quelle que soit la dose quotidienne administrée. Les chercheurs ont également observé une diminution quant aux paramètres d’évaluation secondaires mesurés à l’imagerie – y compris le nombre de lésions et la présence de lésions nouvelles ou agrandies à la 24e semaine – parmi les participants traités par l’ozanimod, comparativement au groupe placebo. L’essai clinique RADIANCE a ensuite fait l’objet d’une prolongation, qui a donné lieu à des travaux de phase III auprès de 1 313 participants dans 147 centres de recherche répartis dans 21 pays. Sur une période de deux ans, ces personnes ont reçu soit de l’ozanimod (0,5 mg ou 1 mg) quotidiennement, soit une injection hebdomadaire d’interféron bêta-1a (Avonex), soit un placebo. Dans le cadre de cette étude de phase III, les deux doses d’ozanimod ont réduit le taux annualisé de poussées comparativement à l’interféron bêta-1a, remplissant ainsi le principal critère d’évaluation.
Étude SUNBEAM : essai clinique de phase III
L’objectif des auteurs de l’étude SUNBEAM, essai clinique de phase III aléatoire et à double insu, consistait à comparer, durant 12 mois, l’efficacité et l’innocuité de l’ozanimod (administré à 0,5 mg ou à 1 mg) à celles de l’interféron bêta-1a. L’ozanimod a rempli le principal critère d’évaluation en réduisant le taux annualisé de poussées par rapport à l’interféron bêta-1a. En comparaison de ce dernier, l’ozanimod a aussi permis une réduction du nombre de lésions nouvelles ou agrandies.
À l’issue d’une analyse prédéfinie de l’ensemble des données recueillies lors des essais de phase III RADIANCE et SUNBEAM relativement au temps écoulé jusqu’à l’aggravation confirmée de l’incapacité, il est ressorti que les groupes traités par l’ozanimod présentaient un taux très faible de progression de l’incapacité. Toutefois, les résultats obtenus auprès des participants ayant reçu ce médicament n’ont pas atteint le seuil de signification statistique comparativement à l’Avonexmd.
Étude de prolongation
Celgene mène actuellement une étude de prolongation de phase III en mode ouvert auprès de personnes qui ont participé à des essais antérieurs sur l’ozanimod. Ainsi, les participants peuvent continuer à prendre l’ozanimod pendant cinq années supplémentaires. Les effets secondaires à long terme issus de cette étude de prolongation seront révélés au milieu de 2020.
La Food and Drug Administration (FDA – Secrétariat américain aux produits alimentaires et pharmaceutiques) a rejeté la demande d’homologation de l’ozanimod pour le traitement des personnes atteintes de SP cyclique déposée par Celgene, car les données présentées étaient insuffisantes pour l’examen du nouveau médicament.
Effets secondaires signalés
Les effets indésirables les plus fréquemment rapportés relativement au groupe traité lors de l’essai clinique de phase II RADIANCE sont les suivants : maux de tête, rhinopharyngite (inflammation du nez et de la gorge), infections urinaires et infections des voies respiratoires supérieures. Davantage de données sur les effets indésirables de l’ozanimod devraient être tirées des études de phase III menées sur ce médicament. Celgene a signalé que l’innocuité du médicament évaluée lors de l’essai clinique SUNBEAM était comparable à celle relevée lors de l’essai RADIANCE. La Société de la SP veillera à diffuser toute nouvelle information à ce sujet.
Référence
COHEN, J. et coll. « Safety and efficacy of the selective sphingosine 1‑phosphate receptor modulator ozanimod in relapsing multiple sclerosis (RADIANCE): a randomised, placebo-controlled, phase 2 trial », Lancet, 2016; 15(4): 373‑81.